
Signalsequenz
Die Signalsequenz, auch Signalpeptid oder Transitpeptid ist eine Abfolge von Aminosäuren eines Proteins. Diese Aminosäuresequenz entscheidet über den Bestimmungsort, den Transportweg des Proteins innerhalb der Zelle und die Sekretionseffizienz.[1][2]
Vorkommen und Bedeutung
Signalsequenzen finden sich typischerweise bei Proteinen, deren Bestimmungsort sich außerhalb der Zelle, in Biomembranen oder in Kompartimenten befindet. So ist für den Transport in das Endoplasmatische Retikulum, Chloroplasten, Mitochondrien, die Peroxisomen oder den Zellkern und deren Membranen meist eine Signalsequenz erforderlich. Durch Kombination verschiedener Signalsequenzen ist es möglich, dass Proteine gleichzeitig in unterschiedliche Organellen importiert werden, wie etwa Mitochondrium und Chloroplast.[3]
Obwohl Bakterienzellen nicht kompartimentiert sind, können bakterielle Proteine Signalsequenzen besitzen. Diese können die Proteine für den Transport in die Zellmembran oder den Extrazellularraum bestimmen.[4]
Zielkompartimente
Endoplasmatisches Retikulum
Ein Transport in das Lumen oder die Membran des Endoplasmatischen Retikulums (ER) kann während der Proteinbiosynthese erfolgen (cotranslationaler Proteintransport) oder erst als fertiges Protein, das vorher im Zytoplasma hergestellt worden ist (posttranslationaler Proteintransport). Proteine mit hydrophileren Signalsequenzen werden bevorzugt posttranslational transportiert.
Proteine mit hydrophoberen Signalsequenzen werden dagegen cotranslational transportiert. Dies geschieht am „rauen ER“, das mit Ribosomen besetzt ist. Der Transportmechanismus ist komplex und umfasst neben dem Ribosom und der daran gebundenen mRNA auch interagierende Proteine wie der Signalerkennungspartikel (SRP) und ribosomen-assoziierte Proteine. Außerdem wird ein SRP-Rezeptor sowie der Tunnelproteinkomplex (SEC-Komplex, Translocon) in der Membran des ER benötigt.
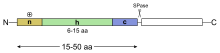
Alle sekretorischen Proteine und die meisten in die Membran integrierten Proteine haben eine Signalsequenz von einer Länge von 15 bis 50 Aminosäuren an ihrem N-Terminus mit bestimmten Eigenschaften.[5][6] Auch innerhalb eines Proteins oder am C-Terminus lassen sich Signalsequenzen finden.
Die genaue Abfolge der einzelnen Aminosäuren ist dabei weniger wichtig, als ihre physikalischen Eigenschaften: ein zentraler hydrophober Kern (h) wird N-terminal (n) von positiv geladenen Aminosäuren und C-terminal (c) von polaren Aminosäuren flankiert. Der C-terminale Bereich enthält oft helixbrechende Aminosäuren wie Prolin oder Glycin. Der N-terminale Bereich ist am wenigsten konserviert. In den meisten Fällen wird die Signalsequenz nach dem Membrandurchtritt vom eigentlichen Protein durch die Signalpeptidase (SPase) abgespalten. Die Schnittstelle wird durch kleine, ungeladene Aminosäurereste in den Positionen −3 und −1 der C-terminalen polaren Region der Signalsequenz definiert.
Die Aminosäuresequenz KDEL sorgt für einen Transport des Proteins in das Endoplasmatische Retikulum und eine Retention darin, bei sekretorischen Proteinen mit KDEL-Sequenz wird im ER die Signalsequenz durch Proteolyse abgespalten, da sie sonst unter anderem durch die Proteine KDELR1, 2 und 3 zurückgehalten werden.
Besonderheiten
Bei manchen Transmembranproteinen ist die erste Transmembrandomäne gleichzeitig die Signalsequenz. Das auch als Signalankersequenz bezeichnete Segment zeichnet sich durch einen längeren hydrophoben Kernbereich sowie eine fehlende Signalpeptidaseschnittstelle gegenüber der normalen Signalsequenz aus.
Der Großteil der Proteine, die zum ER transportiert werden, besitzt N-terminal orientierte Signal- oder Signalankersequenzen. Jedoch gibt es auch integrale Membranproteine, die ohne N-terminale Signalsequenz in die ER-Membran inseriert werden. Bei diesen Proteinen erfolgt die Erkennung über ein C-terminal gelegenes hydrophobes Segment. Wie diese Proteine in die ER-Membran inserieren, ist bisher jedoch noch nicht geklärt.
Zellkern
Auch beim posttranslationalen Proteinimport in den Zellkern ist eine Signalsequenz, hier Kernlokalisierungssignal (prototypische Sequenz PKKKRKV) genannt, erforderlich. Diese wird von einem Kernimportrezeptor erkannt mit diesem zusammen in den Kern transportiert.[7][8] Der Export von Proteinen aus dem Zellkern erfolgt anhand einer NES (engl. nuclear export signal) über Exportine und Ran-GTP mit einem G-Protein-typischen Mechanismus. Das NES besteht aus der Sequenz LxxxLxxLxL mit L stellvertretend für aliphatische Aminosäuren wie Leucin und x für eine beliebige Aminosäure.
Mitochondrium
Der Proteinimport in das Mitochondrium erfolgt posttranslational, also nach abgeschlossener Proteinbiosynthese. Alle Importprozesse erfolgen über die gleiche Transportmaschinerie, den TOM-Komplex (englisch: translocase of the outer membrane) der äußeren Mitochondrienmembran. Daneben bestehen eine Reihe anderer Proteinkomplexe, die die Integration von Proteinen in die äußere Mitochondrien-Membran (SAM-Komplex, sorting and assembly machinery), den Import in die innere Mitochondrienmembran und die Mitochondrienmatrix (TIM-Komplexe, translocase of the inner membrane) vermitteln.
Proteinvorläufer können in zwei Gruppen eingeteilt werden: die erste Gruppe bilden Proteine mit N-terminalen Signalen, die für die Mitochondrien-Matrix bestimmt sind, einige Proteine der inneren Membran und des Intermembranraums zwischen äußerer und innerer Membran. Die Aminosäurereste tragen positive Ladungen und interagieren mit den Importrezeptoren des Organells und leiten es auch über die innere Membran zu ihrem Bestimmungsort. Sie bestehen im Allgemeinen aus 20–40 Aminosäuren, die eine amphiphile α-Helix bilden, die vom Importapparat erkannt wird. Die Signalsequenz wird nach erfolgtem Import durch eine Peptidase abgeschnitten.
Die zweite Gruppe umfasst alle Proteine der äußeren Membran, viele Proteine der inneren Membran und des Intermembranraums. Sie tragen lediglich interne Signale, die nicht abgeschnitten werden können.[9]
Chloroplast
Der Proteinimport in den Chloroplasten erfolgt posttranslational über die Proteinkomplexe TOC (Translocase of the outer chloroplast membrane) und TIC (Translocase of the inner chloroplast membrane).[10]
Plastidäre Signalpeptide befinden sich am N-Terminus des Proteinvorläufers und besitzen bestimmte physikalische Eigenschaften: sie sind reich an Aminosäuren mit hydroxylierten Resten, besitzen keine sauren Reste und bilden keine Sekundärstruktur. Die Präsequenz wird phosphoryliert und geht Interaktionen mit den Proteinen Hsp70 und 14-3-3 ein, die das Protein zum Transportapparat begleiten.[11] Nach dem Import wird die Signalsequenz durch eine Peptidase abgeschnitten. Die Proteine der äußeren Membran erfordern kein N-terminales Signalpeptid, der Mechanismus der Integration ist noch unbekannt.
Proteine, deren Bestimmungsort die Membran oder das Lumen der Thylakoide sind, können ebenfalls zusätzliche Signalsequenzen enthalten.[10]
Peroxisom
Der posttranslationale Proteinimport in das Peroxisom beruht auf zwei unterschiedlichen Arten von Signalsequenzen, die PTS1 und PTS2 genannt werden (von engl.: Peroxisome Targeting Signal, etwa „auf Peroxisomen zeigende Signale“).
PTS1-Sequenzen sind kurze, C-terminale Signale, die die Aminosäureabfolge von (S/A/C)-(K/R/H)-(L/L/M) enthalten. Sie werden von dem Rezeptor Peroxin-5 (Pex5p) erkannt.[12]
PTS2-Sequenzen sind Signale aus 9 Aminosäuren, die etwa 20 Residuen vom N-Terminus entfernt liegen. Der Rezeptor für PTS2-Signale ist des Peroxin-7 (Pex7p).[12]
Literatur
- Lincoln Taiz, Eduardo Zeiger: Physiologie der Pflanzen. Spektrum Akademischer Verlag, Heidelberg 2000, ISBN 3-8274-0537-8.
- Figueroa-Martinez et al.: Reconstructing the Mitochondrial Protein Import Machinery of Chlamydomonas reinhardtii. In: Genetics. vol. 179 (1), 2008, S. 149–155.
- Joachim Rassow et al.: Duale Reihe der Biochemie. Thieme Verlag, Stuttgart 2006, ISBN 3-13-125351-7.
Einzelnachweise
- ↑ L. Kober, C. Zehe, J. Bode: Optimized signal peptides for
the development of high expressing CHO cell lines. In: Biotechnol. Bioeng.
Band 110,
Nr. 4, April 2013,
S. 1164–1173,
doi:
 10.1002/bit.24776,
10.1002/bit.24776,
 PMID 23124363.
PMID 23124363.
- ↑ G. von Heijne: Signal sequences: The limits of variation.
In: J Mol Biol. Band 184,
Nr. 1, Juli 1985,
S. 99–105,
doi:
 10.1016/0022-2836(85)90046-4,
10.1016/0022-2836(85)90046-4,
 PMID 4032478.
PMID 4032478.
- ↑ Alexander Levitan u. a.:
 Dual targeting of the protein disulfide isomerase RB60 to the chloroplast and the endoplasmic reticulum.
In: Proc Natl Acad Sci U S A. 102 (17), 2005, S. 6225–6230
Dual targeting of the protein disulfide isomerase RB60 to the chloroplast and the endoplasmic reticulum.
In: Proc Natl Acad Sci U S A. 102 (17), 2005, S. 6225–6230  doi:10.1073/pnas.0500676102
doi:10.1073/pnas.0500676102
- ↑ Susana Cristóbal u. a.: Competition between Sec-and TAT-dependent protein translocation in Escherichia coli.
In: EMBO J. 18 (11), 1999, S. 2982–2990.
 doi:10.1093/emboj/18.11.2982
doi:10.1093/emboj/18.11.2982
- ↑ G. Blobel, B. Dobberstein: Transfer of proteins across membranes. I. Presence of proteolytically processed and
unprocessed nascent immunoglobulin light chains on membrane-bound ribosomes of murine myeloma. In:
Journal of Cell Biology. 67 (3), 1975, S. 835–851.
 PDF (freier Volltextzugriff, engl.)
PDF (freier Volltextzugriff, engl.)
- ↑ B. Martoglio, B. Dobberstein: Signal sequences: more than just greasy peptides. In:
Trends Cell Biol. 8 (10), 1998, S. 410–415.
 PMID 9789330;
PMID 9789330;
 doi:10.1016/S0962-8924(98)01360-9
doi:10.1016/S0962-8924(98)01360-9
- ↑ X. Xu, I. Meier: The nuclear pore comes to the fore. In: Trends Plant Sci. 13 (1), 2008, S. 20–27
 doi:10.1016/j.tplants.2007.12.001
doi:10.1016/j.tplants.2007.12.001
- ↑ Allison Lange u. a.: Classical Nuclear Localization Signals: Definition, Function, and Interaction with
Importin. In: J Biol Chem. 282 (8), 2006, S, S. 5101–5105
 doi:10.1074/jbc.R600026200
doi:10.1074/jbc.R600026200
- ↑ N. Wiedemann u. a.: The protein import machinery of mitochondria. In:
J Biol Chem. 279 (15), 2004, S. 14473–14476.
 PMID 14973134
PMID 14973134
- ↑ Hochspringen nach: a b
M. Gutensohn u. a.: Toc, Tic, Tat u. a.: Structure and function of protein transport machineries in chloroplasts. In: J Plant Physiol. 163 (3), 2006, S. 333–347
 doi:10.1016/j.jplph.2005.11.009
doi:10.1016/j.jplph.2005.11.009
- ↑ Jürgen Soll, Enrico Schleiff: Plant cell biology: Protein import into chloroplasts. In: Nat Rev Mol Cell Biol. vol. 5, (3), 2004, S. 198–208.
- ↑ Hochspringen nach: a b L. A. Brown, A. Baker:
Peroxisome biogenesis and the role of protein import. In: J Cell Mol Med. 7 (4), 2003, S. 388–400.
 PMID 14754507
PMID 14754507


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 14.09. 2024