
Disulfiram
| Sicherheitshinweise | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||
| MAK | DFG/Schweiz: 2 mg/m3 (gemessen als einatembarer Staub)[1][4] | ||||||||||
| Toxikologische Daten | 500 mg/kg (LD50, Ratte, oral)[5] | ||||||||||
Disulfiram (INN), auch Tetraethylthiuramdisulfid (TETD), (Handelsname Antabus®) ist ein Arzneistoff, der zur Unterstützung der Abstinenz bei Alkoholabhängigkeit angewendet werden kann.
| Strukturformel | ||
|---|---|---|
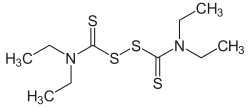
| ||
| Allgemeines | ||
| Freiname | Disulfiram | |
| Andere Namen |
| |
| Summenformel | C10H20N2S4 | |
| Kurzbeschreibung | farblose Kristalle[1] | |
| Externe Identifikatoren/Datenbanken | ||
| CAS-Nummer | | |
| EG-Nummer | 202-607-8 | |
| ECHA-InfoCard | | |
| PubChem | | |
| DrugBank | | |
| Arzneistoffangaben | ||
| ATC-Code | | |
| Wirkmechanismus | Hemmung der Aldehyddehydrogenasen | |
| Eigenschaften | ||
| Molare Masse | 296,54 g/mol−1 | |
| Aggregatzustand | fest[1] | |
| Dichte | 1,30 g/cm3 [1] | |
| Schmelzpunkt | 70 °C[1] | |
| Siedepunkt | 117 °C (22,7 mbar)[1] | |
| Löslichkeit | wenig löslich in Wasser (0,2 g/l bei 20 °C), löslich in Ethanol, Aceton, Diethylether, Benzol, Trichlormethan, Schwefelkohlenstoff[1] | |
Alkoholismus
Wirkung
Normalerweise wird in der Leber der aufgenommene Alkohol über die Zwischenstufe Acetaldehyd zur Essigsäure umgewandelt, ähnlich wie bei der Essigherstellung durch Gärung. In diesen Abbau des Alkohols greift nun das Medikament ein und verhindert den letzten Schritt zur Umwandlung in die Essigsäure durch Blockade des Enzyms Aldehyddehydrogenase. Die Folge ist, dass sich Acetaldehyd anreichert. Dieses bewirkt das sogenannte Acetaldehydsyndrom, welches darin besteht, dass, sobald Alkohol auch in geringen Dosen eingenommen wird, starke und unangenehme Unverträglichkeitsreaktionen entstehen, wie Hautrötung, Kältegefühl in den Armen und Beinen, Übelkeit, Kopfschmerzen und vor allem Herzrasen und Blutdruckabfall bis hin zum Herz-Kreislauf-Schock. Hierdurch kann jedoch bei gefährdeten Personen sogar Herzenge (Angina pectoris) und ein Herzinfarkt ausgelöst werden.
Entsprechende Arzneimittel werden als Tabletten verabreicht. Es kann auch als Depotpräparat unter die Haut implantiert werden.[6]
Gefahren
Da die angesprochenen Unverträglichkeitsreaktionen bei Einnahme größerer Alkoholmengen sogar tödlich sein können (Acetaldehyd ist giftig), werden disulfiramhaltige Präparate nur noch selten und bei solchen Patienten angewandt, bei denen von guter Mitarbeit bei der Behandlung ausgegangen werden kann.[7] Außerdem darf dieses Medikament nur bei genauer Vorabklärung gegeben werden, z. B. nicht bei schwerem Leberschaden.
Siehe auch
Diverse Antibiotika, einige Antidiabetika und weitere Medikamente sowie das Pilzgift Coprin haben in Kombination mit Alkohol die gleiche Wirkung wie Disulfiram (Acetaldehydsyndrom).[1]
Onkologie
Als im Rahmen von Forschungen in den 2010er Jahren die Wirkung von Disulfiram untersucht worden ist, entdeckte man eine antikarzinogene Wirkung mit potentieller Einsatzmöglichkeit als Medikament gegen Krebs.[8][9][10][11][12][13]
Eine epidemiologische Studie an Dänen aus dem Jahr 2014 zeigte, dass Menschen, die aufgrund einer Alkoholabhängigkeit Disulfiram einnahmen, seltener an Brust- oder Prostatakrebs erkrankten. Eine Risikoreduktion für Melanom ergab sich in der Studie hingegen nicht.[14]
Präklinische Studien zeigen, dass Disulfiram in vitro das Wachstum von Tumorzellen der männlichen Prostata hemmt. Auch im Mäusemodell reduzierte das Medikament die Tumorwachstumsrate um bis zu 40 %, konnte sie jedoch nicht vollständig hemmen.[15] In-vitro-Studien an Brustkrebszellen ergaben, dass Disulfiram bei Tumorzellen, nicht aber bei gesunden Zellen der Brust, eine Apoptose induziert.[16] Eine Wirkung von Disulfiram wurde auch auf Tumorzellen bei nicht-kleinzelligem Lungenkrebs und beim Glioblastom gefunden. DSF ist demnach vielversprechend für die Behandlung von Hirntumoren, weil es die BHS überwinden kann und das Wachstum von Hirntumoren hemmt. Es sind jedoch weitere Studien erforderlich, um zu verstehen, wie effektiv diese Wirkung ist.[17][18]
Der genaue Mechanismus dieser Wirkung auf Krebszellen ist nicht bekannt und wird noch untersucht. Eine Rolle dürfte die Bildung von Komplexen des aktiven Metaboliten, Ditiocarb, der in der Leber aus Disulfiram gebildet wird, mit Kupfer spielen. Disulfiram zeigt eine bessere Wirksamkeit auf die Wachstumshemmung von Tumorzellen, wenn es in Kombination mit Kupfer verabreicht wird.[19]
Es gibt zum heutigen Zeitpunkt (Dezember 2017) erst eine klinische Studie an 40 Patienten mit nicht-kleinzelligem Lungenkrebs, in der eine Gruppe zusätzlich zu einer Chemotherapie Disulfiram erhielt und mit einer Gruppe, die nur Chemotherapie erhielt, verglichen wurde. In der Gruppe mit Disulfiram kam es zu einer Erhöhung der mittleren Überlebensdauer von 7.1 auf 10 Monate. Die Aussagekraft dieser Studie ist jedoch durch die kleine Fallzahl limitiert; weitere klinische Studien werden durchgeführt.[20]
Sonstige Verwendung
Disulfiram dient als Hilfsmittel bei der Vulkanisation von Gummi. Historisch interessant ist der von 1937 überlieferte Bericht des Werksarztes, dem die alkoholaversive Wirkung erstmals bei Arbeitern in diesem Bereich zufällig auffiel, wobei diese dem strukturanalogen Tetramethylthiuramdisulfid und dessen Monosulfid ausgesetzt waren.[21][22]
Einzelnachweise
- ↑ Hochspringen nach: a b c d e f g h Eintrag zu Tetraethylthiuramdisulfid. In: Römpp Online. Georg Thieme Verlag.
- ↑ Hochspringen nach: a b Eintrag zu
 Disulfiram in der
GESTIS-Stoffdatenbank des Institut für Arbeitsschutz der Deutschen Gesetzlichen Unfallversicherung. (JavaScript erforderlich)
Disulfiram in der
GESTIS-Stoffdatenbank des Institut für Arbeitsschutz der Deutschen Gesetzlichen Unfallversicherung. (JavaScript erforderlich)
- ↑ Eintrag zu
 Disulfiram im
Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA).
Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung
Disulfiram im
Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA).
Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung
 erweitern.
erweitern.
- ↑ Schweizerische Unfallversicherungsanstalt (Suva):
 Grenzwerte – Aktuelle MAK- und BAT-Werte
(Suche nach 97-77-8 bzw. Disulfiram).
Grenzwerte – Aktuelle MAK- und BAT-Werte
(Suche nach 97-77-8 bzw. Disulfiram).
- ↑ Eintrag zu
 Disulfiram in der Datenbank der United States National Library of Medicine
(NLM)
Disulfiram in der Datenbank der United States National Library of Medicine
(NLM)
- ↑ Fachinformation für Antabus im Arzneimittelkompendium der Schweiz.
- ↑ Emminger, H. Thomas, K. EXAPLAN Band 2; 6. Aufl.; S. 2141.
- ↑ Boris Cvek in: Drug Repurposing for Terminal-Stage Cancer Patients. American Journal of Public Health, Vol. 106, No. 6, June 2016, S. e3-e3.
- ↑ Diethyldithiocarbamate complexes with metals used as food supplements show different effects in cancer cells, with Jindřich Sedláček (Palacky University, Olomouc), Luisa M.D.R.S. Martins (ISEL Lisbon / Technical University Lisbon, Portugal) Petr Daněk (Palacky University, Olomouc), Armando J.L. Pombeiro (Technical University Lisbon, Portugal), Journal of Applied Biomedicine, Vol. 12, No. 4, November 2014, S. 301–308.
- ↑ Nonprofit drugs as the salvation of the world's healthcare systems: the case of Antabuse (disulfiram). Drug Discovery Today 2012.
- ↑ Antabuse repurposing: we need more knowledge and wide international support. International Journal of
Cancer 2011
The Ubiquitin-Proteasome System (UPS) and the Mechanism of Action of Bortezomib, with Dvořák Z., Current Pharmaceutical Design 2011. - ↑ Targeting Malignancies with Disulfiram (Antabuse): Multidrug Resistance, Angiogenesis, and Proteasome. Current Cancer Drug Targets (IF = 4,327) 2011.
- ↑ Antabuse (disulfiram) as a pilot case of nonprofit drug. International Journal of Cancer 2010.
- ↑ Gro Askgaard, Søren Friis, Jesper Hallas, Lau C. Thygesen, Anton Pottegård: Use
of disulfiram and risk of cancer. In: European Journal of Cancer Prevention.
Band 23,
Nr. 3,
S. 225–232,
doi:
 10.1097/cej.0b013e3283647466.
10.1097/cej.0b013e3283647466.
- ↑ Kristiina Iljin, Kirsi Ketola, Paula Vainio, Pasi Halonen, Pekka Kohonen:
High-Throughput Cell-Based Screening of 4910 Known Drugs and Drug-like Small Molecules Identifies Disulfiram as an Inhibitor of Prostate Cancer Cell
Growth. In: Clinical Cancer Research.
Band 15,
Nr. 19, 1. Oktober 2009, S. 6070–6078,
doi:
 10.1158/1078-0432.ccr-09-1035.
10.1158/1078-0432.ccr-09-1035.
- ↑ Di Chen, Qiuzhi Cindy Cui, Huanjie Yang, Q. Ping Dou: Disulfiram, a clinically used
anti-alcoholism drug and copper-binding agent, induces apoptotic cell death in breast cancer cultures and xenografts via inhibition of the proteasome activity. In:
Cancer Research. Band 66,
Nr. 21, 1. November 2006,
S. 10425–10433,
doi:
 10.1158/0008-5472.CAN-06-2126,
10.1158/0008-5472.CAN-06-2126,
 PMID 17079463.
PMID 17079463.
- ↑ Lincan Duan, Hongmei Shen, Guangqiang Zhao, Runxiang Yang, Xinyi Cai: Inhibitory
effect of Disulfiram/copper complex on non-small cell lung cancer cells. In: Biochemical and Biophysical Research Communications.
Band 446,
Nr. 4,
S. 1010–1016,
doi:
 10.1016/j.bbrc.2014.03.047.
10.1016/j.bbrc.2014.03.047.
- ↑ Joanna Triscott, Mary Rose Pambid, Sandra E. Dunn: Concise Review: Bullseye:
Targeting Cancer Stem Cells to Improve the Treatment of Gliomas by Repurposing Disulfiram. In: STEM CELLS. Band 33,
Nr. 4, 1. April 2015,
S. 1042–1046,
doi:
 10.1002/stem.1956.
10.1002/stem.1956.
- ↑ Zdenek Skrott, Martin Mistrik, Klaus Kaae Andersen, Søren Friis, Dusana Majera:
Alcohol-abuse drug disulfiram targets cancer via p97 segregase adaptor NPL4. In: Nature.
Band 552,
Nr. 7684, Dezember 2017,
doi:
 10.1038/nature25016.
10.1038/nature25016.
- ↑ Gro Askgaard, Søren Friis, Jesper Hallas, Lau C. Thygesen, Anton Pottegård: Use
of disulfiram and risk of cancer. In: European Journal of Cancer Prevention. Band 23, Nr. 3,
S. 225–232,
doi:
 10.1097/cej.0b013e3283647466.
10.1097/cej.0b013e3283647466.
- ↑ Helge Kragh: FROM DISULFIRAM TO ANTABUSE: THE INVENTION OF A DRUG. In:
Bull. Hist. Chem. Band 33,
Nr. 2, 2008 (
 illinois.edu [PDF]).
illinois.edu [PDF]).
- ↑ Disulfiram. MAK Value Documentation in German language, 1997. In:
The MAK-Collection for Occupational Health and Safety. Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim, Germany 31. Januar 2012,
S. 1–34,
doi:
 10.1002/3527600418.mb9777d0024.
10.1002/3527600418.mb9777d0024.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 01.03. 2026


