
Glucose-1-phosphat
| Sicherheitshinweise | |||||||
|---|---|---|---|---|---|---|---|
| |||||||
D-Glucose-1-phosphat (auch Cori-Ester genannt) ist die am Kohlenstoffatom C1 phosphorylierte Form von D-Glucose und ein Isomer von D-Glucose-6-phosphat. In vielen Stoffwechselschritten spielt es eine wichtige Rolle.
Biologische Bedeutung
Glucose-1-phosphat ist in verschiedenen Stoffwechselwegen involviert. Im Glykogenstoffwechsel wird es aus Glykogen durch phosphorolytische Spaltung gebildet, was eine Glycogenphosphorylase katalysiert. Durch Isomerisierung kann Glucose-1-phosphat in Glucose-6-phosphat für eine weitere Prozessierung isomerisiert werden, diese Reaktion ist reversibel und wird von einer Phosphoglucomutase katalysiert. Darüber hinaus dient G1P zur Biosynthese extrazellulärer Polysaccharide.[3]
| Strukturformel | ||
|---|---|---|
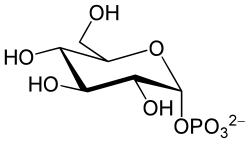
| ||
| Deprotonierte Form von α-D-Glucose-1-phosphat | ||
| Allgemeines | ||
| Name | Glucose-1-phosphat | |
| Andere Namen | ||
| Summenformel | C6H13O9P | |
| Kurzbeschreibung | Farbloser Feststoff (Kaliumsalz)[2] | |
| Externe Identifikatoren/Datenbanken | ||
| CAS-Nummer | ||
| EG-Nummer | 200-435-8 | |
| ECHA-InfoCard | | |
| PubChem | | |
| ChemSpider | | |
| DrugBank | | |
| Eigenschaften | ||
| Molare Masse | 260,14 g/mol | |
Eine weitere, wichtige Reaktion ist die Bildung von UDP-Glucose aus α-D-Glucose-1-phosphat und
UTP durch eine UTP-Glucose-1-phosphat-Uridyltransferase (GULT; UDP-Glucose-Phosphorylase EC
![]() 2.7.7.9):
[4]
2.7.7.9):
[4]
UDP-Glucose spielt nicht nur eine Rolle im Glykogenstoffwechsel, sondern auch im Galactosestoffwechsel und im Uronsäurenstoffwechsel.
Neben UTP können auch andere Nukleotide wie dTTP, ATP,
CTP und GTP mit Glucose-1-phosphat verknüpft werden.
Katalysiert werden diese Reaktionen durch verschiedene Transferasen (EC
![]() 2.7.7.24, EC
2.7.7.24, EC
![]() 2.7.7.27, EC
2.7.7.27, EC
![]() 2.7.7.33 bzw. EC
2.7.7.33 bzw. EC
![]() 2.7.7.34).
2.7.7.34).
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Eintrag zu
 DISODIUM GLUCOSE PHOSPHATE
in der CosIng-Datenbank der EU-Kommission, abgerufen am 2. September 2025.
DISODIUM GLUCOSE PHOSPHATE
in der CosIng-Datenbank der EU-Kommission, abgerufen am 2. September 2025.
- ↑ Hochspringen nach: a b Datenblatt
 α-D-Glucose 1-phosphate dipotassium salt hydrate, BioXtra, ≥98% bei Sigma-Aldrich">Sigma-Aldrich, abgerufen am 2. September 2025.
(
α-D-Glucose 1-phosphate dipotassium salt hydrate, BioXtra, ≥98% bei Sigma-Aldrich">Sigma-Aldrich, abgerufen am 2. September 2025.
(  SDB).
SDB).
- ↑ Dai, J. et al. (2006): Conformational cycling in beta-phosphoglucomutase catalysis: reorientation of the beta-D-glucose 1,6-(Bis)phosphate intermediate. In:
Biochemistry 45(25); 7818–7824;
 PMID 16784233;
doi:
PMID 16784233;
doi:  10.1021/bi060136v
10.1021/bi060136v
- ↑ Jan Kolmann und Klaus-Heinrich Röhm: Taschenatlas der Biochemie. 3., vollständig überarbeitete und erweiterte Auflage 2003, Stuttgart, Georg Thieme Verlag, ISBN 978-3137594031; S. 156f.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 02.11. 2025